人工智能如何助力小分子药物开发 基础软件的创新引擎
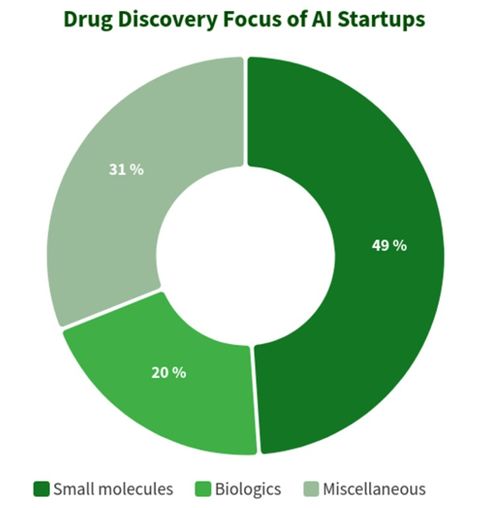
在当今生物医药领域,人工智能正以前所未有的深度和广度,重塑小分子药物开发的传统范式。这一变革的核心驱动力之一,便是人工智能基础软件的快速发展。它们不仅加速了药物发现的进程,更在降低研发成本、提高成功率方面展现出巨大潜力。
一、人工智能基础软件:药物研发的“智能大脑”
人工智能基础软件为药物研发提供了强大的计算和分析平台。这些软件通常集成了机器学习、深度学习、自然语言处理以及生成式模型等先进技术。它们能够处理和分析海量的化学、生物学和临床数据,包括化合物结构、蛋白质靶点信息、高通量筛选结果、基因组学数据和已发表的科学文献。通过算法模型,这些软件可以识别人类难以察觉的复杂模式和关联,从而成为药物化学家和生物学家不可或缺的“智能大脑”。
二、赋能小分子药物发现的关键环节
- 靶点识别与验证:AI软件可以整合多组学数据(基因组、转录组、蛋白组等),预测与疾病相关的新颖药物靶点,并评估其“成药性”,帮助研究人员在早期锁定最有希望的干预目标。
- 化合物虚拟筛选与生成:这是AI应用最活跃的领域之一。传统的“试错法”高通量筛选成本高昂、效率有限。AI软件,特别是基于深度学习和生成对抗网络的模型,能够:
- 虚拟筛选:快速从数百万甚至数十亿的虚拟化合物库中,预测出与靶点蛋白结合最有可能的候选分子,大幅缩小实验验证的范围。
- 从头药物设计:根据靶点蛋白的三维结构或特性,直接“生成”具有理想理化性质、高亲和力和选择性的全新分子结构,突破了已知化学空间的限制。
- 化合物优化:对初步筛选出的先导化合物,AI软件可以预测其ADMET(吸收、分布、代谢、排泄和毒性)性质,指导化学家对分子结构进行定向优化,提高其成药性,减少后期开发失败的风险。
- 化学反应与合成路径预测:AI模型可以预测化学反应的可行性、产率以及最优合成路径,加速从分子设计到实际合成的过程,解决药物化学中的合成挑战。
三、典型的人工智能基础软件工具
市场上已涌现一批有影响力的AI药物发现软件和平台,例如:
- Schrödinger的“薛定谔平台”:集成了基于物理的计算和机器学习方法,用于分子建模、虚拟筛选和结合自由能计算。
- Atomwise的AtomNet®:利用卷积神经网络进行基于结构的药物发现。
- BenevolentAI的知识图谱平台:整合海量生物医学数据,构建关联网络,用于靶点发现和机制理解。
- Insilico Medicine的Chemistry42:一个生成式强化学习平台,专门用于生成和优化新型小分子。
- 开源工具:如DeepChem、RDKit等,也为学术界和工业界提供了强大的AI药物发现基础框架和化学信息学工具包。
四、挑战与未来展望
尽管前景广阔,AI驱动的小分子药物开发仍面临挑战:数据质量与标准化、模型的可解释性(“黑箱”问题)、以及最终仍需湿实验验证的“最后一公里”问题。
人工智能基础软件的发展将呈现以下趋势:
- 多模态与融合:更深度地整合化学、生物学、影像学、临床文本等多模态数据。
- 模型专业化与精准化:针对特定靶点家族(如GPCR、激酶)或疾病领域开发更专业的模型。
- 自动化与闭环:将AI设计、虚拟验证、自动化合成与高通量测试更紧密地结合,形成“设计-制造-测试-学习”的智能化闭环迭代系统。
- 云计算与平台即服务:基于云端的AI药物发现平台将降低使用门槛,使更多研究机构能够利用顶尖的计算资源和技术。
人工智能基础软件正成为小分子药物开发的革命性工具。它们通过提升从靶点到候选药物的各个环节的效率和精准度,有望将药物发现的“十年磨一剑”缩短为更可控的周期,最终为患者带来更多创新疗法。这场由软件驱动的创新,标志着药物研发正全面迈入数据与智能双轮驱动的新时代。
最新产品

华为与开发者的“情谊” 在HDC.Cloud 2021上书写智能时代新篇
航天宏图新设子公司布局AI软件开发 加速人工智能领域技术落地

从“星环”到星河 星环科技如何以技术之光点亮人工智能软件开发的未来

G60研究院举办新能源与汽车零部件行业智能化技术改造培训班,聚焦AI基础软件实战应用
化企仪表以“稳”得天下!仪表运维现状及未来展望,另附我国智能工厂进程展望及人工智能基础软件开发

PTC发布Creo 11 人工智能赋能新一代基础软件开发平台
大数据与人工智能发展趋势及前景 人工智能基础软件的突破与展望
重磅 2017年人工智能行业现状与发展趋势报告——聚焦基础软件开发
AI新航向 阿尔特曼眼中的未来,软件基石与去手机化的智能世界

解锁机器学习实战 星环科技人工智能基础软件开发秘籍问世